中国科学院上海植物生理生态研究所等在阻断疟疾传播研究中取得重大进展
文章来源: | 发布时间:2017-10-11 | 【打印】 【关闭】
2017年9月29日,国际权威学术期刊《科学》(Science) 在线发表了中国科学院上海植物生理生态研究所王四宝研究组合作完成的题为“Driving mosquito refractoriness to Plasmodium falciparum with engineered symbiotic bacteria”的最新研究论文。该研究首次发现了能在按蚊中进行持续跨代传播的新共生细菌,成功构建了抗疟效应分子高效分泌表达系统,攻克了驱动抗疟基因在蚊群中快速渗透的关键难题,为抗击疟疾提供强大的新“武器”。
蚊子作为媒介传播疟疾、登革热、黄热病和寨卡等多种重大传染病,严重威胁人类的健康。其中,以按蚊为传播媒介的疟疾最为严重,发病率和死亡率始终居高不下。全球每年有2-3亿人感染,年死亡人数近百万,平均每1-2分钟就有一名儿童死于疟疾,全世界约一半人口面临疟疾风险。随着全球化和人员往来的频繁,近年我国输入性疟疾病例呈显著上升趋势。
疟疾是由雌性按蚊叮咬而感染疟原虫所引起的虫媒传染病。全球近500种按蚊中,约有100种是疟疾的适宜传播媒介。蚊媒防制一直是阻断疾病传播的主要措施。然而,蚊虫对化学农药已产生普遍抗性,研发新的对抗疟疾传播方法迫在眉睫。该研究团队此前发展了由肠道共生菌介导的阻止蚊子传播疟疾的方法—转基因共生菌(Paratransgenesis),即通过遗传改造手段,使肠道共生菌成为抗疟基因表达载体,分泌表达抗疟蛋白,高效专一地杀灭按蚊体内的疟原虫,从而有效阻断疟疾传播(Wang et al., PNAS, 2012)。但是,Paratransgenesis策略与利用转基因蚊阻断疟疾传播方法一样,仍面临巨大挑战—如何驱动抗疟基因快速渗透到整个蚊群中?
本项研究攻克了这一关键难题。王四宝研究团队从按蚊体内分离到兼具垂直和水平传播能力的沙雷氏菌属新菌株Serratia sp. (AS1),经过多年努力成功构建了抗疟效应分子高效分泌表达系统,使其成为活菌“疫苗”或抗疟药物的双重载体,实现在多种按蚊体内高效抑制恶性疟原虫(Plasmodium falciparum),不受按蚊种间或种群间存在生殖隔离的限制;研究发现该共生菌能由雄蚊通过交配水平传播给雌蚊,还可通过粘附在卵壳表面经雌蚊产卵垂直传给后代蚊虫,实现持续跨代传播。同时,该共生菌不影响蚊虫寿命,具有生态环境安全性。这项研究为抗疟基因快速渗透到整个蚊群提供了一个安全高效的驱动系统,有望成为阻断疟疾传播的新的防治策略,具有广阔的应用前景。未来将进行现场试验,加速推动成果转化。该策略也为防控其它蚊虫媒介传染病(登革热、寨卡等)和植物虫媒病害提供了崭新思路。
该项研究由王四宝研究组与美国约翰霍普金斯大学Marcelo Jacobs-Lorena教授研究组合作完成。中国科学院上海植物生理生态研究所为第一完成单位。该研究得到了中科院战略性先导科技专项 (B类)、国家自然科学基金、中科院“人才计划”和美国国家过敏和传染病研究所等项目资助。
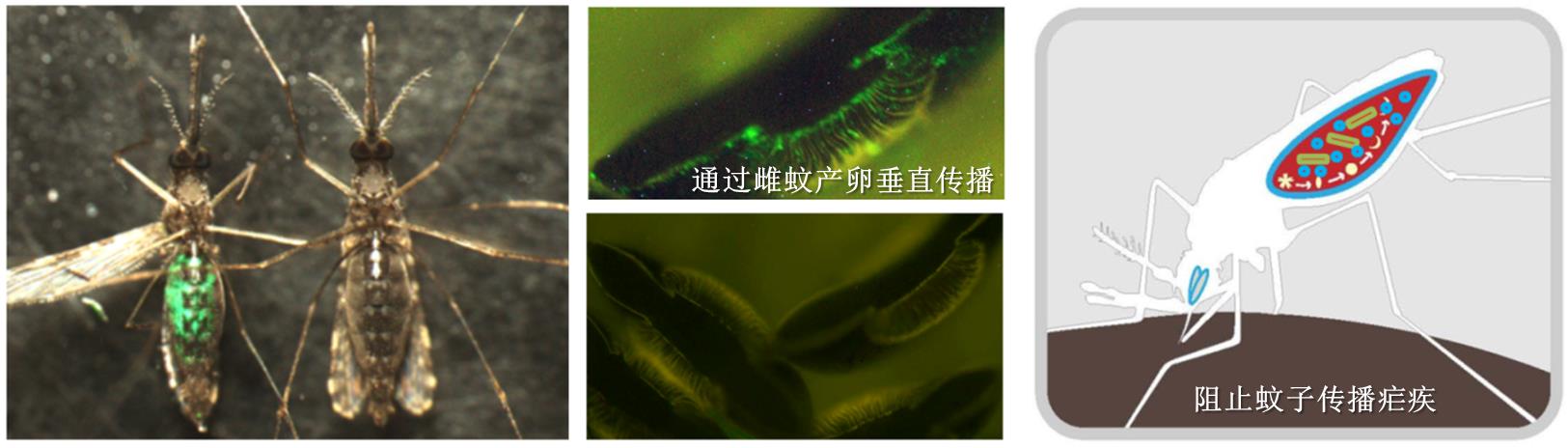
中科院上海植生生态所等发现能在按蚊中进行持续跨代传播的新共生细菌,能高效驱动抗疟效应分子快速散播到整个蚊群中,阻止蚊子传播疟原虫。
