生化与细胞所创建更为精准的谱系示踪技术
文章来源: | 发布时间:2017-11-28 | 【打印】 【关闭】
11月13日,国际学术期刊 Nature Medicine 在线发表了中国科学院生物化学与细胞生物学研究所周斌研究组的科研成果“Enhancing the precision of genetic lineage tracing using dual recombinases ”。该研究将Dre-rox同源重组系统引入到传统的基于Cre-loxP同源重组系统的遗传谱系示踪技术中,有效地规避了由于Cre表达的不特异性而导致的非特异性(“异位”)同源重组,实现了更为精准的遗传谱系示踪,为发育、干细胞及再生等领域的深入研究奠定了可靠的技术基础。
遗传谱系示踪技术是揭示特定类型细胞在发育、疾病和再生中转分化现象的有效 研究方法,目前,体内的细胞追踪技术主要基于 Cre-loxP 同源重组系统。在含有 Cre 的转基因小鼠中,Cre 由于在特性基因的启动子驱动下,表达在特定的细胞类群中,当 Cre 小鼠与含有 loxP 位点的报告基因小鼠交配时,Cre 通过识别 loxP 位点,将两个 loxP 位点之间的终止序列切除,从而使含有 Cre 的细胞类群表达出报告基因,由于这种切除是位于基因上的,从而是永久性的和不可逆的,因此,所有表达 Cre 的细胞类群及其后代(无论是否表达 Cre)都将永久的被报告基因蛋白标记上,因此,利用该细胞追踪技术可以解析特定细胞的起源和命运。
尽管基于 Cre-loxP 系统的遗传谱系示踪技术是研究发育、疾病、再生等过程细胞命运可塑性的强大利器,但是它本身也存在着技术瓶颈。该技术的准确性主要依赖于 Cre 表达的特异性,如果有微量的 Cre 表达在了非靶向细胞中即为所谓的异位表达,那么谱系示踪结果的可靠性将大大降低,而这也成为了近年来很多科学问题出现争议的主要原因之一。
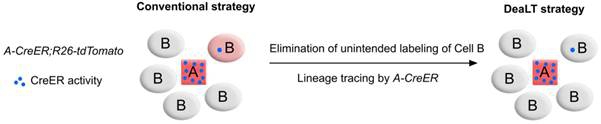
为了解决这一技术瓶颈,何灵娟博士等在周斌研究员指导下开发了一种新的谱系示踪技术称之为DeaLT (Dual-recombinase-activated lineage tracing),该技术将Dre-rox同源重组系统与传统的Cre-loxP同源重组系统结合起来,Dre-rox 介导的同源重组反应在可能引起 Cre 异位表达的细胞中将Cre重组酶的识别位点 loxP 切除掉,从而有效地阻止了 Cre-loxP 的异位同源重组,增加了 Cre-loxP 介导的谱系示踪结果的准确性。该系统包含两种策略,分别是DeaLT-IR 和DeaLT-NR。DeaLT-IR策略的报告基因小鼠上包含的两个loxP位点和两个rox位点以交错形式存在(loxP-rox-loxP-rox),该策略适合组成性Dre与诱导性Cre相结合;而DeaLT-NR策略报告基因小鼠上的loxP位点和rox位点以嵌合的形式存在(rox-loxP-loxP-rox),该策略适合诱导性Dre和诱导性Cre相结合。
系统创建成功后,周斌组研究人员首先利用DeaLT-IR策略解决了成体心脏 c-Kit+心脏干细胞的问题。成体 c-Kit+干细胞是否能够分化形成心肌细胞之所以存在争议主要是由于 c-Kit 除了表达在非心肌细胞中以外,本身还微量地表达在心肌细胞中,传统的示踪技术利用Kit-CreER无法做到单纯示踪c-Kit+干细胞,而利用新开发的DeaLT系统阻断了心肌细胞中Kit-CreER的同源重组反应,成功的实现了非心肌细胞中 c-Kit+干细胞特异性的遗传谱系示踪。他们的结果发现,c-Kit+干细胞在成体心脏生理稳态和损伤修复过程中均不会分化形成心肌细胞,主要是通过血管新生参与心脏修复。 此外,利用 DeaLT-NR系统他们解决了肝脏领域有关 Sox9+肝组细胞能否转分化形成肝细胞的争议问题,造成该争议的主要原因是 Sox9 除了表达在胆管上皮细胞中还少量的表达在了胆管周围的肝细胞里面,传统的谱系示踪技术利用Sox9-CreER标记了胆管上皮细胞和胆管周围的一部分肝细胞,因此很难判断损伤后Sox9-CreER标记的新生成的肝细胞到底来自哪一部分。DeaLT技术阻断了Sox9-CreER在肝细胞中的同源重组反应,实现了 Sox9+胆管上皮细胞中特异性的遗传谱系示踪,结果发现在肝脏生理稳态和损伤修复过程中 Sox9+胆管上皮细胞并不会转分化形成肝细胞。DeaLT策略不仅提供更精确的Cre重组酶的控制,并且为Cre表达细胞的谱系追踪设定了更高的技术标准,但同时它也足够灵敏以检测体内谱系转换事件。以肝损伤后肝细胞转分化形成胆管上皮细胞为例,DeaLT策略能够清楚地展现肝损伤后肝细胞能够转分化形成胆管上皮细胞的过程。因此,这种新策略可用于揭示细胞命运转变,同时也严格控制潜在的非靶向细胞表达Cre介导的异位谱系追踪,为多个研究领域更准确地解析细胞起源和命运提供了有效的手段。
该研究得到了生化与细胞所季红斌研究员,北京生命科学研究所陈婷教授、上海交通大学附属国际和平妇幼保健院黄荷凤教授,波士顿儿童医院William Pu教授,复旦大学附属中山医院颜彦教授、阜外医院的胡盛寿及聂宇教授、中国医学科学院血液研究所韩忠朝及韩之波教授、暨南大学蔡冬青教授、同济大学费俭教授等大力帮助和支持。该研究工作得到了中科院、基金委、科技部以及上海科委等经费支持。