近日,在《Neuron》期刊在线发表的研究揭示了α‑突触核蛋白病理传播过程中的新关键因素——“柔性衣壳”(fuzzy coat)。该研究由中国科学院上海有机化学研究所、中国科学技术大学的研究人员合作完成,为深入理解帕金森病、路易体痴呆等神经退行性疾病的传播机制提供了新视角。
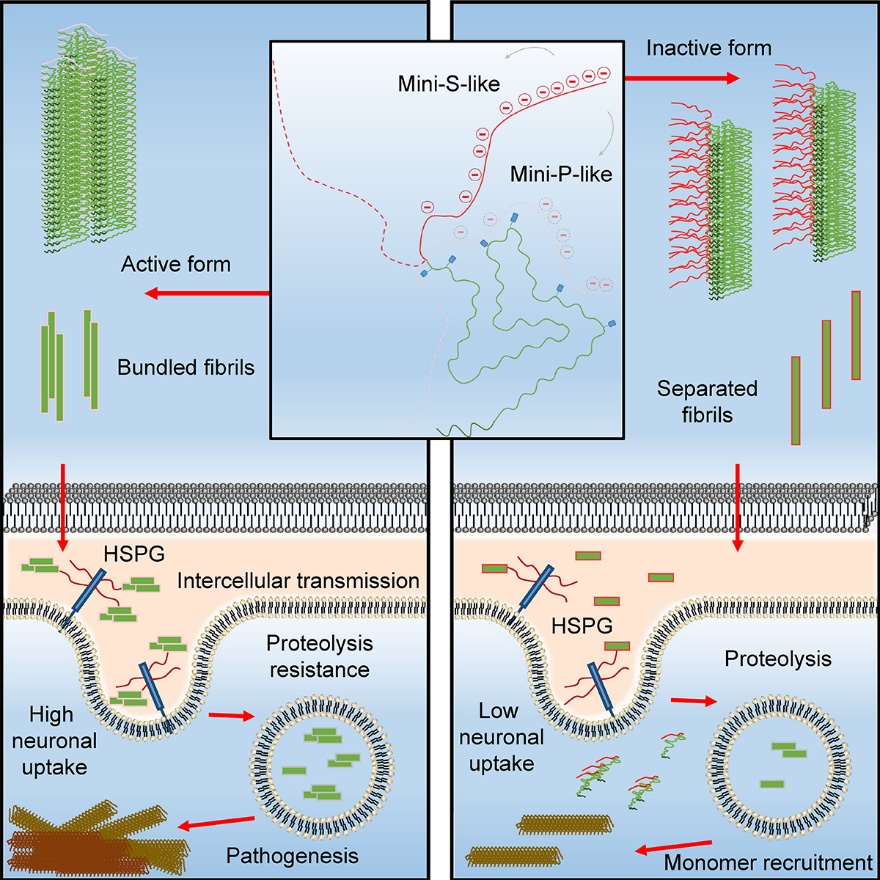
研究团队利用α‑突触核蛋白预制纤维(preformed fibrils,PFF)作为病理种子,通过体外反复扩增的方式模拟病理蛋白在大脑内的传播过程。实验中,他们发现原始种子经过连续扩增后,其神经传递活性呈逐渐下降趋势。进一步的分析揭示,在α‑突触核蛋白纤维中存在两种不同的多态性:一种为Mini‑P型,另一种为Mini‑S型。两者的纤维核心结构基本相似,但在包裹纤维核心的“柔性衣壳”上存在显著差异。Mini‑P型纤维的柔性衣壳较为紧凑,部分屏蔽了负电荷,而Mini‑S型则呈现出相对松散的状态。
利用冷冻电镜(cryo‑EM)、固体核磁共振(ssNMR)以及氢/氘交换质谱(HDX‑MS)等前沿技术,研究人员精细解析了这两种纤维在柔性区的差异。结果表明,紧凑的Mini‑P型纤维由于屏蔽了部分负电荷,可以更有效地与神经元表面的受体——硫酸乙酰肝素蛋白聚糖(HSPG)结合,从而更容易被神经元摄取。此外,这种结构也使其对蛋白酶的降解具有更高的抵抗力,延长了细胞内的半衰期。相反,Mini‑S型纤维虽然在体外能更快地募集单体形成纤维,但其较松散的柔性衣壳导致神经元致病活性较低。
这项研究的重要意义在于,它首次将目光从传统关注的纤维核心转向了纤维外部柔性区域,揭示了“柔性衣壳”在病理蛋白传播中的关键作用。研究人员通过构建模型表明,α‑突触核蛋白在体内的传播过程可能正是由于这一柔性区域结构的微妙调控所致。为验证这一观点,团队还利用了构象特异性抗体,这些抗体能够区分Mini‑P型和Mini‑S型纤维,并在来自路易体病、帕金森病和伴痴呆患者的脑组织中检测到类似的病理模式,进一步证明了这一机制在人体内同样适用。
该研究不仅加深了人们对神经退行性疾病病理传播机制的理解,也为未来的治疗策略指明了方向。相较于传统的清除所有病理蛋白的策略,针对纤维柔性衣壳的精准干预或许能更有效地降低病理种子的传播活性,从而减缓疾病进程。这一新发现为开发更具针对性的治疗药物提供了理论依据,同时也有望成为早期诊断和疾病进展评估的重要生物标志物。
总之,这项研究成果,凭借其将结构生物学和神经病理学方法交叉创新应用,不仅为揭示α‑突触核蛋白病理传播的分子机制提供了新线索,更为神经退行性疾病的精准治疗带来了全新的希望。随着后续研究的深入,针对“柔性衣壳”的干预策略有望成为未来治疗帕金森病等神经退行性疾病的重要突破口。
本研究由中国科学院上海有机化学研究所生物与化学交叉研究中心研究员贺焯皓、刘聪博士以及中国科技大学项晟祺教授为共同通讯作者;交叉中心韩雨良,夏文程以及中科大李娟博士为共同第一作者。本研究获中国科学院、中国国家自然科学基金、科技部重点研发计划、上海市科委等项目支持。