9月19日,国际学术期刊Cell Research在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)刘珈泉研究组联合中国科学院上海免疫与感染研究所钟劲研究组的最新研究成果:"ATP-dependent one-dimensional movement maintains immune homeostasis by suppressing spontaneous MDA5 filament assembly"。研究团队通过单分子荧光成像技术,系统性地揭示了MDA5蛋白作为ATP驱动的分子马达在双链RNA上进行易位运动的分子机制,阐明了这种独特的运动方式如何抑制MDA5纤丝状寡聚体(filament)的组装以维持免疫稳态,为理解先天免疫调控和自身免疫疾病机制提供了全新视角。
MDA5是RIG-I样受体(RLR)家族的重要成员,负责识别病毒双链RNA并启动先天免疫反应,其激活需要沿着双链RNA形成filament状结构,从而触发N端CARD结构域的寡聚化。虽然已知MDA5的ATP酶活性对维持免疫稳态至关重要,可能通过调节纤维组装实现,但其潜在的分子机制一直不清楚。这一问题的解决,将深化我们对先天免疫调控机制的理解。
为探究MDA5的工作机制,研究团队利用单分子荧光成像技术首次直接观察并实时追踪了MDA5蛋白在双链RNA上的动态行为,并结合负染电镜、生化分析和细胞免疫学实验等多种方法,深入解析MDA5 filament组装的调控机制。研究团队发现,MDA5作为ATP水解驱动的分子马达,能够沿着双链RNA进行一维运动。多个MDA5马达可以协同加载到单条双链RNA上,但它们的运动很少同步,这种不同步的运动有效抑制了自发的filament形成和激活。
更重要的是,研究团队揭示了LGP2作为MDA5信号传导关键调节因子的新机制。LGP2能够识别运动中的MDA5马达并阻止其运动,从而通过"运动阻断机制"促进microfilament组装。这种独特的组装策略突出了一维运动在高阶蛋白寡聚化中的重要作用,并揭示了维持免疫稳态的新颖机制。
这项研究不仅在理论上丰富了我们对先天免疫受体工作机制的认识,还为自身免疫疾病的治疗提供了新的靶点。研究团队对已知与人类自身免疫疾病相关的MDA5 ATP酶缺陷突变体(R337G和M854K)进行了研究,发现这些突变体失去了正常的一维运动能力,导致对自身RNA的异常识别和免疫反应。这一发现为理解相关自身免疫疾病的发病机制提供了关键的分子基础,也为开发针对先天免疫系统精准调控的新型治疗策略奠定了重要基础。
分子细胞卓越中心刘珈泉研究员和中国科学院上海免疫与感染研究所钟劲研究员为该论文的共同通讯作者。分子细胞卓越中心博士研究生韩晓鹏、博士后饶铭、中国科学院上海免疫与感染研究所博士研究生常钰为共同第一作者。该工作得到分子细胞卓越中心陈玲玲研究员、侯法建研究员、张少庆研究员的大力支持,以及中国科学院战略性先导科技专项、国家重点研发计划、核糖核酸功能与应用重点实验室和国家自然科学基金的资助。
文章链接:https://doi.org/10.1038/s41422-025-01183-8
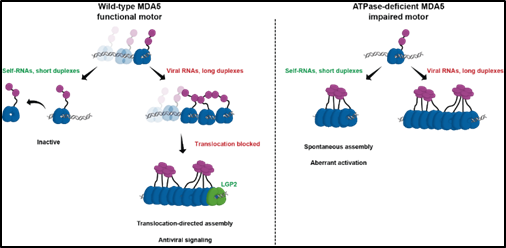
MDA5通过ATP依赖的一维运动维持免疫稳态的分子机制

